آرتمیسینین و مشتقات نیمه مصنوعی آن گروهی از داروها هستند که در درمان مالاریای ایجاد شده توسط انگل پلاسمودیوم فالسیپاروم مورد استفاده قرار می گیرند.
این دارو سال 1972 توسط یویو تو کشف شد، دانشمند برجسته ای که در زمینه شیمی و داروسازی فعالیت می کند و سال 2015 برای کشف و تحقیق روی آرتمیسینین جایزه نوبل پزشکی دریافت کرده است.
درمان های مبتنی بر آرتمیسینین یا ACT ها در حال حاضر درمان استاندارد برای مالاریای ایجاد شده توسط انگل پلاسمودیوم فالسیپاروم و سایر گونه های پلاسمودیوم در سراسر جهان محسوب می شوند.
این ماده از گیاه افسنطین شیرین که جزو گیاهان دارویی شناخته شده در طب چینی می باشد استخراج می شود، همچنین می توان یک ترکیب پیش ساز از آن را با کمک مخمر مهندسی ژنتیک تولید کرد که بسیار موثرتر از استفاده از گیاه می باشد.
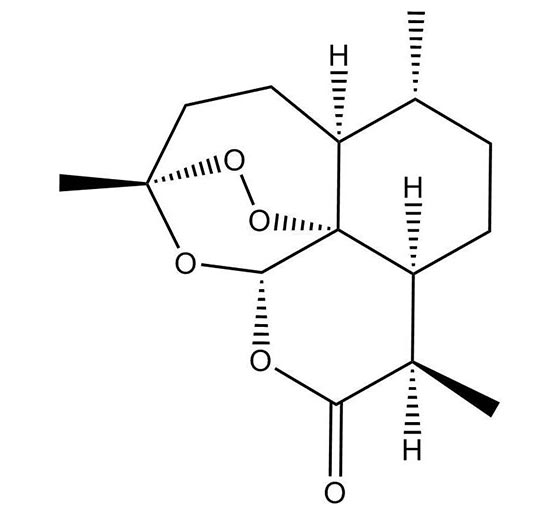
آرتمیسینین و مشتقات آن که همگی لاکتون های سس کوئی ترپن حاوی یک پل پراکسید غیر معمول می باشند (این حلقه تریوکسان اندوپراکسید 1، 2، 4 عامل خواص ضد مالاریایی آرتمیسینین است) برای درمان عفونت های کرم انگلی و مالاریا استفاده می شوند و نسبت به سایر داروها قادر به کشتن هر چه سریع تر و مختل کردن همه مراحل چرخه زندگی انگل ها هستند.
اگرچه فراهمی زیستی پایین، خواص فارماکوکینتیکی ضعیف و هزینه بالای تولید آن ها از مشکلات موجود بر سر راه استفاده از آن ها می باشد.
لازم به ذکر است سازمان بهداشت جهانی استفاده از این داروها را به عنوان تنها روش درمانی مالاریا چندان توصیه نمی کند زیرا اخیرا نشانه هایی مبنی بر مقاوم شدن احتمالی انگل مالاریا در برابر این دارو گزارش شده است. به نظر می رسد روش های درمانی ترکیب شده از آرتمیسینین یا مشتقات آن با برخی داروهای ضد مالاریای دیگر نتیجه بهتری به دنبال داشته باشد.
استفاده پزشکی
در حال حاضر سازمان بهداشت جهانی، داروی آرتمیسینین یا یکی از مشتقات آن (معمولا در ترکیب با یک داروی همراه طولانی اثر) را به عنوان خط مقدم درمان برای همه انواع مالاریا توصیه می کند.
در مورد مالاریای بدون عوارض، سازمان بهداشت جهانی 3 روز مصرف خوراکی یکی از پنج درمان مبتنی بر آرتمیسینین (که در ادامه ذکر شده) را توصیه کرده است :
- آرتمتر + لومفانترین
- آرتسونات + آمودیاکین
- آرتسونات + مفلوکین
- دی هیدرو آرتمیسینین + پیپرازین
- آرتسونات + سولفادوکسین پریمتامین
هنگام استفاده از هر یک از ترکیبات ذکر شده، مشتق آرتمیسینین به سرعت انگل مالاریا را از بین می برد اما خود نیز بسیار سریع از بدن پاک می شود، به همین دلیل استفاده از داروهای طولانی اثر به همراه این ترکیبات توصیه شده تا این داروها علاوه بر از بین بردن انگل های باقی مانده، محافظت طولانی مدت در برابر عود احتمالی عفونت ایجاد کنند.
در مورد نمونه های شدیدتر مالاریا، به توصیه سازمان بهداشت جهانی درمان درون وریدی یا عضلانی با داروی آرتسونات مشتق شده از آرتمیسینین به مدت حداقل 24 ساعت انجام می شود. درمان مبتنی بر آرتسونات تزریقی تا زمانی که بیمار قادر به مصرف داروهای خوراکی نباشد ادامه پیدا می کند، سپس یک دوره 3 روزه مصرف داروهای ACT تجویز می شود که مشابه درمان مالاریای بدون عوارض می باشد.
در صورتی که آرتسونات در دسترس نباشد تزریق عضلانی داروی ضعیف تر آرتمتر مشتق شده از آرتمیسینین توصیه می شود. در کودکان کمتر از 6 سال، اگر آرتسونات تزریقی در دسترس نباشد از نسخه مقعدی استفاده شده و پس از آن لازم است کودک به مراکز مجهزتر انتقال داده شود.
استفاده از آرتمیسینین ها به دلیل عمر بسیار کوتاه (نیمه عمر) آن ها برای پیشگیری از مالاریا توصیه نمی شود، زیرا برای اثر بخشی لازم است چند بار در روز تجویز شوند.
موارد منع مصرف
به دلیل عدم تحقیقات کافی در مورد ایمنی آرتمیسینین در اوایل بارداری، سازمان بهداشت جهانی به خانم های باردار توصیه کرده از مصرف داروهای ACT در سه ماه اول بارداری اجتناب کنند و به جای آن یک دوره 7 روزه مصرف کلیندامایسین و کینین را تایید کرده است. این در حالیست که برای سه ماه دوم و سوم بارداری دوره درمان معمولی با داروهای ACT در نظر گرفته شده است.
برای برخی گروه های خاص نیز مصرف ACT ها به دلیل عوارض جانبی داروهای همراه آن ها در درمان مالاریا توصیه نمی شود، به عنوان مثال :
- مصرف سولفادوکسین – پیریمتادین در چند هفته اول زندگی به دلیل تداخل در عملکرد بیلی روبین و تشدید زردی نوزاد مجاز نمی باشد
- در افراد مبتلا به اچ آی وی مثبت ترکیب تری متوپریم / سولفامتوکسازول، درمان های ضد رتروویروس حاوی زیدوودین و همچنین ASAQ (آرتسونات + آمودیاکین) با نوتروپنی مرتبط است
- به نظر می رسد ترکیب داروی افاویرنز برای اچ آی وی و ASAQ با مسمومیت کبدی رابطه داشته باشد
عوارض جانبی
به طور کلی گفته شده مصرف آرتمیسینین در دوزهای مورد استفاده برای درمان مالاریا به خوبی توسط بدن تحمل می شود.
عوارض جانبی گروه دارویی آرتمیسینین مشابه علائم مالاریا است که شامل حالت تهوع، استفراغ، از دست دادن اشتها و سرگیجه می باشد. در برخی موارد ممکن است ناهنجاری های خفیف خون نیز مشاهده شود.
یکی از عوارض جانبی نادر اما جدی در مصرف این داروها واکنش های آلرژیک است. همچنین یک مورد التهاب شدید کبدی در مورد استفاده طولانی مدت از دوز نسبتا بالای آرتمیسینین گزارش شده که دلایل آن مشخص نیست (بیمار به مالاریا مبتلا نبوده است).
داروهایی که در درمان های ترکیبی استفاده می شوند ممکن است احتمال بروز عوارض جانبی در افرادی که تحت درمان هستند را افزایش دهند. عوارض جانبی در افرادی که به مالاریای حاد ناشی از انگل پلاسمودیوم فالسیپاروم مبتلا هستند و تحت درمان با مشتقات آرتمیسینین قرار می گیرند بیشتر است.
شیمی دارویی
مولکول های آرتمیسینین دارای یک جز غیر معمول به نام حلقه تریوکسان اندوپراکسید 1، 2، 4 هستند که عامل ضد مالاریای اصلی مولکول ها محسوب شده و تغییرات در موقعیت کربن 10 باعث ایجاد مشتقات قوی تر از ترکیب اصلی می شود.
از آن جا که اثر بخشی آرتمیسینین به دلیل برخی خصیصه های فیزیکی آن مانند فراهمی زیستی ضعیف محدود می شود، مشتقات نیمه مصنوعی آرتمیسینین ایجاد شده است که از جمله آن ها می توان به مشتقات دی هیدرو آرتمیسینین اشاره کرد. همچنین مشتقات آرتسونات، آرتیتر و آرتمتر اولین بار در سال 1986 سنتز شدند.
تاکنون مشتقات دیگری نیز تولید شده که آرتلینیک اسید، آرتموتیل، آرتمسین، SM735، SM905، SM933، SM934 و SM1044 قوی ترین آن ها محسوب می شوند.
در توسعه پیش بالینی نیز تشابهات ساده ای وجود دارد. به علاوه بیش از 120 مشتق دیگر نیز ایجاد شده که آزمایش بالینی روی آن ها به دلیل عدم حمایت مالی امکان پذیر نبوده است.
از آن جا که آرتمیسینین در روغن و آب کمتر حل می شود، معمولا به صورت گوارشی (به صورت خوراکی یا مقعدی) تجویز می شود اما آرتسونات را می توان به صورت داخل وریدی، عضلانی و همچنین خوراکی و مقعدی استفاده کرد.
علاوه بر این تست آزمایشگاهی روی یک ترکیب مصنوعی با ساختار تری اکسولان مشابه (حلقه ای حاوی سه اتم اکسیژن) به نام RBx-11160 نتایج امید بخشی به دنبال داشته و با این که آزمایش فاز دوم آن روی بیماران مبتلا به مالاریا به اندازه مورد انتظار موفقیت آمیز نبود تولید کنندگان تصمیم گرفتند فاز سوم را شروع کنند.
مکانیسم عمل
آرتمیسینین خود نوعی پیش دارو برای دی هیدرو آرتمیسینین فعال بیولوژیکی است. این متابولیت در داخل اریتروسیت ها دچار شکاف حلقه اندوپراکسید می شود.
زمانی که مولکول های دارو با هِم (که با هموگلوبین گلبول های قرمز خون ارتباط دارد) تماس پیدا می کنند، اکسید آهن II حلقه اندوپراکسید را می شکند. این فرایند باعث تولید رادیکال های آزاد می شود که به نوبه خود به پروتئین های حساس آسیب رسانده و باعث مرگ انگلی می شود.
سال 2016 مشخص شد که آرتمیسینین به موارد هدف متعدد متصل می شود که یعنی عملکرد بسیار جسورانه ای دارد. بخش اندوپراکسید آرتمیسینین نسبت به اکسید آهن II آزاد حساسیت کمتری است و به همین دلیل در مراحل داخل اریتروسیتی انگل پلاسمودیوم فالسیپاروم فعالیت بیشتری دارد.
این در حالیست که طبق مطالعات بالینی مشخص شده آرتمیسینین بر خلاف سایر داروهای ضد مالاریایی در تمام چرخه زندگی انگل فعال است.
مقاومت دارویی
اولین بار در سال 2008 در منطقه جنوب شرقی آسیا شواهد بالینی مبنی بر مقاومت دارویی انگل مالاریا نسبت به آرتمیسینین گزارش شد و به دنبال آن مطالعات دقیق در کامبوج غربی آن را تایید کرد. پس از آن گزارش های مختلفی در این مورد طی سال های 2012 در تایلند و 2014 در کامبوج، ویتنام و شرق میانمار دریافت شد.
در سال 2014 نیز شواهدی مبنی بر نوعی مقاومت در حال ظهور در جنوب لائوس، میانمار مرکزی و شمال شرقی کامبوج به دست آمد. به نظر می رسد ژن کلچ انگل در کروموزوم 13 نشانگر مولکولی مسئول در ایجاد مقاومت بالینی در جنوب شرقی آسیا می باشد.
سازمان بهداشت جهانی در سال 2011 از این مسئله ابراز نگرانی کرده و اظهار داشت که مقاومت دارویی انگل در برابر موثرترین داروی ضد مالاریا یعنی آرتمیسینین می تواند تمام برنامه های انجام شده طی دهه گذشته که پیشرفت چشمگیری نیز داشته اند را مختل کند.
اگرچه آرتمیسینین به تنهایی قادر به مقابله با انگل مالاریا می باشد اما متاسفانه بعد از بهبود بیماری، انگل ها دوباره و به سرعت برمی گردند و مالاریا عود می کند. برای پاکسازی بدن از تمام انگل ها و جلوگیری از عود بیماری به سایر داروها نیز نیاز می باشد.
سازمان بهداشت جهانی با توجه به این مسئله که مقاومت دارویی انگل مالاریا در برابر آرتمیسیین می تواند فاجعه به دنبال داشته باشد، تولید کنندگان را تحت فشار قرار داده تا از دسترس قرار دادن داروی غیر ترکیبی در اختیار جامعه پزشکی اجتناب کنند.
دو مکانیسم اصلی مقاومتی، مقاومت پلاسمودیوم در برابر داروهای ضد مالاریا را تحریک می کند. اولین مورد مسئله انتشار دارو به نواحی دورتر از ناحیه اثر است که به دلیل جهش در ژن های مختلف ناقل یا افزایش تعداد کپی های ژن رخ می دهد و مورد دوم تغییر در هدف انگلی به دلیل جهش در ژن های مربوطه است.
مقاومت پلاسمودیوم فالسیپاروم به ترکیبات آرتمیسینین جدید با یک مکانیسم جدید مقاومتی در زمینه پدیده سکون ارتباط دارد.
سنتز
بیوسنتز در افسنطین شیرین
تصور می شود بیوسنتز آرتمیسینین شامل مسیر موالونات (MVA) و چرخه فارنسیل دی فسفات (FDP) می باشد. مشخص نیست که آیا مسیر غیر موالونات نیز می تواند به پیش سازهای 5 کربنی کمک کند یا خیر، همان طور که در سایر سیستم های بیوسنتز سسکی ترپن رخ می دهد.
در مورد مسیرهای الکل آرتمیسینیک به آرتمیسینین همچنان بحث های زیادی وجود دارد و اغلب از نظر زمان انجام مرحله کاهش متفاوت هستند. هر دو مسیر دی هیدرو آرتمیسینیک اسید را به عنوان پیش ماده نهایی آرتمیسینین پیشنهاد می کنند، سپس این ماده تحت فتو اکسیداسیون قرار می گیرد تا دی هیدرو آرتمیسینیک اسید هیدرو پراکسید تولید شود.
بیوسنتز آرتمیسینین با انبساط حلقه با تجزیه هیدرو پراکسید و هیدرو پراکسیداسیون با واسطه اکسیژن ثانویه به پایان می رسد.
سنتز شیمیایی
تاکنون بارها سنتز کامل آرتمیسینین از مواد اولیه آلی موجود با استفاده از معرف های آلی اساسی انجام شده است.
اولین سنتز یک سنتز استرو انتخابی توسط اشمید و هوفینز در موسسه هافمن لا روچ در شهر بازل سوئیس با شروع از (-) – ایزوپولگول (13 مرحله، عملکرد کلی ~5%) بوده و دیگری سنتز همزمانی است که توسط ژو و همکارانش در انستیتوی شانگهای شیمی آلی از (R) – (+) – سیترونلال (20 مرحله، عملکرد کلی ~0.3% ) انجام شده است.
مراحل اصلی رویکرد اشمید – هوفینز شامل یک هیدروبراسیون / اکسیداسیون استریو انتخابی اورلوف اولیه برای ایجاد استریو مرکزی متیل خارج از حلقه در زنجیره جانبی پروپن، دو آلکیلاسیون واسطه دار با معرف لیتیوم پی در پی که تمام اتم های کربن مورد نیاز را وارد کند و همچنین مراحل کاهش، اکسیداسیون و دسیلیلاسیون بعدی که روی این واسطه مونو کاربوسیکلیک (شامل یک فتواکسیژناسیون با استفاده از اکسیژن مجرد نهایی و یک واکنش که بعد از روند اسیدی، سه حلقه سیکل باقی مانده محصول مورد نظر یعنی آرتمیسینین را در یک مرحله می بندد) انجام می شود می باشد.
از آن زمان تا امروز طیف گسترده ای از مسیرهای دیگر نیز مورد بررسی قرار گرفته اند که از جمله آن ها می توان به مسیرهای سنتز کامل از (R) – (+) – پولگون، ایزومنتن، و حتی 2 – سیکلو هگزن – 1 – 1 و همچنین مسیرهایی که به صورت جزئی یا نیمه سنتز از یک پیش ماده بیوسنتز فراوان تر یعنی اسید آرتمیسینیک توصیف می شوند.
مورد دوم شامل برخی نمونه های سنتز بیومیمتیک بسیار کوتاه و بسیار پر بازده (از روث و اکتون و هاینز و همکاران، 3 مرحله، عملکرد 30%) می باشد.
سنتز در ارگانیسم های مهندسی شده
توسعه آرتمیسینین نیمه مصنوعی توسط برنامه توسعه دارویی PATH و با بودجه بنیاد بیل و ملیندا گیتس انجام شد. این پروژه سال 2004 و با همکاری اولیه دانشگاه برکلی کالیفرنیا (که فناوری مورد نیاز پروژه را فراهم کرد، فرایندی که به طور ژنتیکی مخمر را برای تولید اسید آرتمیسینیک تغییر داده است) و آمیریس (شرکت بیوتکنولوژی در کالیفرنیا که فرایند را برای تولید گسترده در مقیاس پالایش و فرایندهای مقیاس پذیر برای انتقال به یک شریک صنعتی توسعه داد) آغاز شد.
سال 2006 تیمی از دانشگاه برکلی گزارش دادند که مخمر ساکارومایسس سرویزیه را برای تولید مقدار کمی از اسید آرتمیسینیک پیش ساز مهندسی کرده اند. سپس اسید آرتمیسینیک سنتز شده می تواند منتقل و خالص سازی شده و از نظر شیمیایی به آرتمیسینین تبدیل می شود.
در این تلاش مبتنی بر بیولوژی مصنوعی از یک مسیر اصلاح شده میوالونات استفاده شد و سلول های مخمر برای بیان آنزیم آمورفادین سنتاز و یک سیتوکروم P450 مونوکسیژناز (CYP71AV1)، هر دو از افسنطین شیرین، مهندسی شدند. یک اکسیداسیون سه مرحله ای آمورفا – 4، 11 – دین اسید آرتمیسینیک تولید می کند.
شیوه عمل دانشگاه برکلی با کمک فناوری سازمان های مختلف دیگر تکمیل شد. آخرین فناوری موفق مبتنی بر اختراعات دارای مجوز از دانشگاه برکلی و انستیتوی بیو تکنولوژی گیاهی شورای تحقیقات ملی کانادا است.
هم اکنون تولید تجاری آرتمیسینین نیمه مصنوعی در شرکت سانوفی در جارسیو ایتالیا در حال انجام است. این منبع دوم آرتمیسینین برای فراهم کردن جریان پایدارتری از درمان های ضد مالاریا برای کسانی که بیشترین نیاز را به آن دارند اعلام آمادگی کرده است.
سال 2013 سازمان بهداشت جهانی اعلام کرد استفاده از آرتمیسینین نیمه مصنوعی برای تولید مواد دارویی فعال ارسال شده برای این سازمان جهت ارزیابی یا آن هایی که قبلا تایید شده اند را پذیرفته است. ماده فعال دارویی سانوفی که از آرتمیسینین نیمه مصنوعی تولید می شود نیز در همین سال توسط سازمان بهداشت جهانی ارزیابی و به عنوان اولین مشتق نیمه مصنوعی آرتمیسینین معرفی شد.
سال 2010 تیمی از دانشگاه واخنینگن اعلام کردند که یکی از مواد مرتبط با تنباکو به نام Nicotiana benthamiana را مهندسی کرده و به نظر می رسد می تواند اسید آرتمیسینیک تولید کند.
نحوه تولید و قیمت
در حال حاضر کشورهای چین و ویتنام حدود 70 درصد و آفریقای شرقی حدود 20 درصد ماده گیاهی اولیه این دارو را تامین می کنند.
نهال های افسنطین شیرین ابتدا در گلخانه ها پرورش داده شده و سپس به مزارع منتقل می شوند. حدود 8 ماه طول می کشد تا نهال به بلوغ کامل برسد. در مرحله بعد گیاهان برداشت و برگ آن ها خشک می شود، سپس به کارخانجات ارسال می شوند تا در آن جا با کمک یک حلال (معمولا هگزان) آرتمیسینین استخراج شود.
قیمت آرتمیسینین در بازار دائما در حال نوسان در رنج های بسیار متغیر است که از 120 تا 1200 دلار برای هر کیلوگرم بین سال های 2005 تا 2008 بوده است.
شرکت چینی آرتفارم با ترکیب داروهای آرتمیسینین و پیپراکوین داروی آرتکویک را به بازار عرضه کرده است. در چین و جنوب شرقی آسیا تحقیقات بالینی گسترده ای درباره این دارو انجام شده و از آن در مقیاس وسیع در برنامه ریشه کنی مالاریا در مجمع الجزایر قمر استفاده شده است.
این تلاش ها طی سال های 2007، 2012، 2013 و 2014 به کاهش 95 تا 97 درصدی مالاریا در مجمع الجزایر قمر انجامیده است.
شرکت های نوارتیس و سانوفی نیز بعد از مشورت با سازمان بهداشت جهانی، به صورت غیر انتفاعی دست به تولید داروهای ACT زدند، اما قیمت آن ها نسبت به سایر روش های درمان مالاریا هزینه بر می باشد.
داروی تزریقی آرتسونات توسط شرکت داروسازی چینی Guilin برای درمان مالاریای شدید تولید شده و مورد تایید سازمان بهداشت جهانی قرار گرفته است.
بخش محصولات کشاورزی دانشگاه یورک نیز با کمک تکنیک های اصلاح مولکولی دست به تولید انواع پر بازده افسنطین شیرین زده است.
به علاوه مرکز جهانی جنگل داری موفق به تولید گیاهی ترکیبی به نام A3 شده که می تواند تا ارتفاع 3 متر رشد کرده و 20 برابر بیشتر از انواع وحشی این گیاه آرتمیسینین تولید کند. در شمال غربی موزامبیک، این مرکز به همراه سازمان پزشکی، وزارت کشاورزی و توسعه روستایی در تلاش هستند تا به کشاورزان درباره نحوه پرورش بوته از قلمه و برداشت و خشک کردن برگ ها برای تهیه چای آموزش دهند.
با این حال سازمان بهداشت جهانی استفاده از فراورده های گیاهی افسنطین شیرین از جمله چای را برای پیشگیری و درمان مالاریا توصیه نمی کند.
سال 2013 شرکت سانوفی از راه اندازی تاسیساتی در جارسیوی ایتالیا خبر داد که در زمینه تولید داروی ضد پلاسمودیال در مقیاس وسیع فعالیت می کند. همچنین برنامه های مشارکتی با بودجه بنیاد بیل و ملیندا گیتس در زمینه فرایند جدید تولید دارویی توسط برنامه توسعه دارویی PATH انجام شده که بر اساس یک فرایند بیوسنتز اصلاح شده برای اسید آرتمیسینیک (که در ابتدا توسط جی کیسلینگ طراحی شد) می باشد.
ریشه یابی آرتمیسینین
آرتمیسینین یک لاکتون ضد مالاریای مشتق شده از گیاه چینگهائو (افسنطین شیرین) است که از حدود 2 هزار سال پیش در چین مورد استفاده دارویی قرار گرفته است. لی شیژن در سال 1596 در کتاب خود، چای تهیه شده از این گیاه را برای درمان علائم مالاریا توصیه کرده است.
نام آرتمیسینین از الهه یونانی آرتمیس گرفته شده است، اما تصور می شود بعد از ملکه آرتمیسیا دوم از کاریا، که یک گیاه شناس و محقق دارویی در قرن چهارم قبل از میلاد بود، نام گذاری شده باشد.
کشف آرتمیسینین
گیاه افسنطین شیرین با نام علمی Artemisia annua از گیاهان دارویی است که امروزه در بسیاری از نقاط دنیا یافت می شود و از بیش از 2 هزار سال پیش در طب سنتی چینی به عنوان ماده ضد مالاریا مورد توجه قرار گرفته است.
قدیمی ترین شواهد به دست آمده از کاربردهای این گیاه به 200 سال قبل از میلاد در 52 نسخه خطی کشف شده از ماوانگدوی بر می گردد.
کاربرد ضد مالاریایی این گیاه اولین بار در کتاب چینی راهنمای داروهای تجویزی برای شرایط اضطراری به نام Zhouhou Beiji Fang که در اواسط قرن چهارم میلادی توسط جی هونگ ویرایش شد توصیف شده است. در این کتاب 43 روش درمان برای مالاریا ثبت شده است.
ارتش آزادی بخش خلق سال 1967 یک برنامه تحقیقاتی غربال گری گیاهی تحت برنامه مخفی نظامی با نام رمز Project 523 ترتیب داد که ماموریتش یافتن درمان مناسب برای مالاریا بود. این تحقیقات در سال 1972 به کشف آرتمیسینین در برگ های گیاه افسطنین شیرین منجر شد که افتخار کشف آن به نام یویو تو ثبت شده است.
افسنطین شیرین در لیست حدود 5 هزار داروی چینی که توسط دانشمندان چینی به عنوان نامزدهای آزمایشی برای درمان احتمالی مالاریا فهرست شده بودند قرار داشت.
یویو تو کشف کرد که می توان از فرایند استخراج در دمای پایین برای جداسازی یک ماده ضد مالاریای موثر از گیاه استفاده کرد. او در این کشف خود از یک منبع دارویی گیاهی سنتی چینی (کتاب Zhouhou Beiji Fang) الهام گرفته بود. در این کتاب گفته شده گیاه باید در آب سرد غوطه ور شود.
تیم یویو تو بعدها عصاره مفیدی از گیاه استخراج کردند که نتایج تحقیقات آن ها سال 1979 در مجله پزشکی چین منتشر شد. ماده استخراج شده یک بار تصفیه شده و سرانجام در نقطه ای موفق به استخراج آرتمیسینین خالص از آن شدند.
بررسی سال 2012 نشان داد که درمان های مبتنی بر آرتمیسینین موثرترین دارو برای درمان مالاریا تا آن زمان بوده است. همچنین گزارش شد که این ماده قادر به پاکسازی سریع تر انگل های مالاریا از بدن نسبت به سایر داروها می باشد.
پروژه 523 علاوه بر آرتمیسینین، محصولات دیگری همچون لومفانترین، پیپرازین و پیروناریدین نیز تولید کرد که می توان در ترکیب با این ماده مورد استفاده قرار داد.
اواخر دهه 1990 شرکت نوارتیس یک ثبت اختراع چینی جدید برای درمان ترکیبی با آرتمتر / لومفانترین داشته و اولین درمان های ترکیبی مبتنی بر آرتمیسینین (کورتم) را به سازمان بهداشت جهانی ارائه داد که قیمت آن ها کاهش یافته بود.
سال 2006 و پس از آن که آرتمیسینین به عنوان داروی درمان مالاریا انتخاب شد، سازمان بهداشت جهانی خواستار توقف فوری آماده سازی داروهای آرتمیسینین تک دارویی شد و به جای آن استفاده از ترکیب آرتمیسینین با داروهای مالاریایی دیگر را توصیه کرد تا خطر مقاومت انگلی کاهش پیدا کند.
سال 2015 یویو تو به دلیل کشف آرتمیسینین که میزان مرگ و میر بیماران مبتلا به مالاریا را به میزان قابل توجهی کاهش داده بود نیمی از جایزه نوبل پزشکی سال 2015 را دریافت کرد. نیمه دیگر به طور مشترک به ویلیام سی کمپبل و ساتوشی آمورا برای کشف ایورمکتین اعطا شد.
تحقیقات
درمان های ترکیبی مبتنی بر آرتمیسینین
سازمان بهداشت جهانی چهار ACT دیگر نیز معرفی کرده که اگرچه در آزمایش های بالینی یا منطقه ای مورد استفاده قرار می گیرند اما هنوز شواهد کافی برای تایید و توصیه آن ها در استفاده گسترده و جهانی وجود ندارد :
- آرتسونات / پیروناریدین
- آرترولان / پیپراکوین
- آرتمیسینین / پایه پیپراکوین
- آرتمیسینین / نفتاکوین
هلمینتیازیس
در اوایل دهه 1980 دانشمندان چینی در حین جستجوی داروهای ضد کرم جدید برای تب حلزون به این نتیجه رسیدند که آرتمیسینین در مقابل این کرم ها که دومین عفونت انگلی شایع بعد از مالاریا می باشند موثر می باشد.
آرتمیسینین و مشتقات آن همگی جزو داروهای ضد کرم قوی به شمار می روند. بعدها مشخص شد که آرتمیسینین ها بر علیه طیف وسیعی از ترماتودها از جمله شیستوزوما ژاپونیکوم، اس مانسونی، ﺷﻴﺴﺘﻮزوﻣﺎ ﻫﻤﺎﺗﻮﺑﻴﻮم، کپلک جگر چینی، کپلک جگر گوسفند و کپلک جگر آسیای جنوب شرق فعالیت می کنند.
آزمایش های بالینی نیز در بیماران مبتلا به تب حلزون در آفریقا با موفقیت انجام شده است.
سرطان
آرتمیسینین و مشتقات آن به دلیل اثرات بالقوه ضد سرطانی مورد تحقیق قرار گرفته اند. از سال 2018 تنها تحقیقات بالینی مقدماتی روی اثر مشتقات آرتمیسینین در درمان سرطان های مختلف انجام شده که تاکنون هیچ گونه کاربرد بالینی تایید شده ای وجود نداشته است.
بیماری خود ایمنی
مشتقات آرتمیسینین به دلیل توانایی آن ها در سرکوب واکنش های ایمنی مانند التهاب شناخته شده اند. یکی از این مشتقات SM934 نام دارد که در سال 2015 توسط اداره ملی پزشکی چین جهت آزمایش بالینی برای درمان لوپوس اریتماتوی سیستمیک تایید شد.
آزمایش های حیوانی نتایج خوبی داشته و به نظر می رسد این ماده می تواند زیر مجموعه های سلول T را تنظیم کرده، از فعال شدن سلول های B جلوگیری کند و مانع تولید سیتوکین های التهابی و مسیر انتقال سیگنال NF-κB می شود.
منبع: wikipedia